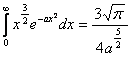Institut für Physikalische und Theoretische Chemie
TU-Braunschweig
- Übungsblatt zur Vorlesung Physikalische
Chemie I
- Thermodynamik, Kinetik -
Sommersemester 2006
Prof. Dr. K.-H. Gericke,
Dipl. Chem. Jan Frähmcke, Dipl. Chem. Sebastian Kauczok
1) Berechnen Sie für He die Wurzel der mittleren
quadratischen Geschwindigkeit (vrms), die mittlere kinetische
Energie und die mittlere Geschwindigkeit für T = 300 K.
2) Gegeben sei die Maxwellverteilung für eine
Komponente des Geschwindigkeitsvektors. Berechnen Sie den Anteil von O2-Molekülen,
die bei einer Temperatur von 500 K eine x-Komponente der Geschwindigkeit
zwischen 300 und 700 ms-1 haben.
Hilfestellung: 
3) Bei der Erdumrundung des Space Shuttles
beobachtete man an dessen Unterseite Leuchterscheinungen, die man sich zunächst
nicht erklären konnte. Zur Aufklärung dieses Phänomens gehen Sie davon aus, dass
das Space Shuttle mit ca. 7,4 km/s die Erde umkreist und dabei auf - als ruhend
angenommene - N2 Moleküle trifft.
a) Wie groß ist die kinetische Energie dieser
Moleküle relativ zur Rakete?
b) Wie groß ist die Temperatur eines N2-Gases, dessen quadratisch
gemittelte Geschwindigkeit <v2>½ gerade der
Geschwindigkeit der Rakete entspricht?
4) Berechnen Sie aus der Boltzmann-Verteilung für
die kinetische Energie eines idealen Gases die wahrscheinlichste Energie, sowie
die mittlere Energie.
Hilfestellung: