Raman-Spektroskopie
![]()
(Original:
http://www.raman.de/html/grundlag.htm)
Die Raman-Spektroskopie beruht auf dem Raman-Effekt. Mit der Raman-Spektroskopie werden die Wellenlängen und die Intensitäten von inelastisch gestreutem Licht gemessen. Das Raman-Streulicht wird bei Wellenlängen beobachtet, das durch Molekül- oder Kristallgitterschwingungen gegenüber dem einfallenden Licht verschoben ist. Im Gegensatz zur Absorption von Molekülschwingungen im infraroten Spektralbereich beruht der Raman-Effekt auf einem anderen physikalischen
Elementarprozess. Jedoch ergänzen sich die Infrarot- und Raman-Spektroskopie in ihrem Informationsgehalt. Anhand von Auswahlregeln kann vorhergesagt werden, welche Schwingungen Infrarot- bzw. Raman-aktiv sind. Typische Anwendungen der Raman-Spektroskopie sind die Strukturbestimmung, die qualitative Analyse von Mehrkomponentensystemen und die quantitative Analyse.
Bestrahlt man Moleküle mit monochromatischem Licht, so wird das eingestrahlte Licht gestreut. Nach Zerlegung des Streulichts zeigen sich neben der intensiven Spektrallinie der Lichtquelle zusätzliche Spektrallinien, die gegenüber der Frequenz der Lichtquelle verschoben sind. Die letzteren Linien nennt man Raman-Linien. Sie sind nach dem indischen Physiker Chandrasekhara Venkata Raman benannt, der im Jahr 1928 als erster über die experimentelle Entdeckung dieser Linien berichtete.
Schematische Darstellung der Energiezustände bei der Rayleigh- und Raman-Streuung. Bei der Raman-Streuung kann die Wellenlänge des eingestrahlten Lichts (grüner Pfeil) entweder zum langwelligen Spektralbereich (Stokes-Raman-Streuung: roter Pfeil) bzw. zum kurzwelligen Spektralbereich (anti-Stokes-Raman-Streuung: blauer Pfeil) verschoben sein. S0, N0: elektronischer bzw. Schwingungsgrundzustand; S1, N1: 1. elektronischer- bzw. schwingungsangeregter Zustand.
Die Wechselwirkung zwischen Materie und Licht kann als ein Stoßvorgang angesehen werden. Dabei ergeben sich drei Möglichkeiten:
1. Beim elastischen Stoß eines Photons mit der Energie hn0 (grüner Pfeil) verändert sich der Energiezustand des Moleküls nicht. Auch die Frequenz der Streustrahlung verändert sich nicht zur Frequenz der Lichtquelle. Diese Streuung wird als Rayleigh-Streuung bezeichnet.
Die beiden anderen Möglichkeiten stellen den Raman-Effekt dar, der als unelastischer Stoß zwischen einem Photon und einem Molekül aufgefaßt werden kann. Die Energie, die dabei abgegeben oder aufgenommen wird, entspricht der Differenz zwischen zwei Energiniveaus einer Molekülschwingung.
2. Das Molekül besitzt nach dem Stoß eine höhere Schwingungsenergie. Das Streulicht ist dabei energieärmer geworden (roter Pfeil) und weist damit eine geringere Frequenz auf. Die beobachtbaren Spektrallinien werden als Stokes-Linien bezeichnet.
3. Das Molekül besitzt nach dem Stoß eine niedrigere Schwingungsenergie. Die Energie des gestreuten Lichts ist dabei größer geworden (blauer Pfeil) und weist eine höhere Frequenz auf. Die beobachtbaren Spektrallinien werden als Anti-Stokes-Linien bezeichnet. Dieser Fall ist nur möglich, wenn das Molekül vor dem Stoß sich in einem höheren Energiezustand befindet.
Anhand von Auswahlregeln kann vorhergesagt werden, welche Schwingungen Infrarot- bzw. Raman-aktiv sind. Da bei der Wechselwirkung von Molekülen mit Photonen der Gesamtdrehimpuls im elektronischen Grundzustand konstant bleiben muß, können nur bestimmte Übergänge induziert werden. Allgemein gilt, daß für ein Molekül mit Symmetriezentrum alle Schwingungen, die symmetrisch zum Symmetriezentrum erfolgen, im IR-Spektrum verboten sind, und alle Schwingungen, die antisymmetrisch sind, im Raman-Spektrum verboten sind. Diese Regel ist als Alternativ-Verbot bekannt.
Eine Infrarot-Absorption wird dann beobachtet, wenn durch die Normalschwingung eine Änderung des Dipolmoments µ im Molekül eintritt. Die Intensität der IR-Schwingungsbande IIR ist proportional zum Quadrat der Änderung des Dipolmoments µ mit der Normalkoordinaten q:
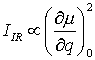
Eine Normalschwingung ist Raman-aktiv, wenn während der Schwingung die Polarisierbarkeit a des Moleküls sich ändert. Die Intensität IRaman einer Raman-Bande ist proportional zum Quadrat der Änderung der Polarisierbarkeit a mit der Normalkoordinaten q:
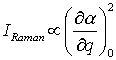
Als Folge der Auswahlregeln kann für organische und biochemisch interessante Moleküle gesagt werden, daß die Infrarot-Spektroskopie mehr über funktionelle Gruppen aussagt und die Raman-Spektroskopie besonders hilfreich für die Charakterisierung des Kohlenstoffgerüsts ist.
Der praktische
Einsatz der Raman-Spektroskopie In der Raman-Spektroskopie können Proben aller Aggregatzustände
untersucht werden, die Messung gasförmiger Substanzen ist jedoch aufgrund der
sehr geringen Dichte schwierig. Das Probenmaterial wird in Glas- oder
Polychlortrifluorethylengefäße (für HF-Lösungen) gefüllt und in den Strahlengang
gebracht. Für temperatur- oder luftempfindliche Chemikalien bietet die
Raman-Spektroskopie den Vorteil das Proben u.U. direkt im Reaktionsgefäß
vermessen werden können. Die Messung selbst wird zum Beispiel so vorgenommen: Eine Justierprobe (z.B. das sehr ramanaktive Schwefel in einem
Glasröhrchen mit 4 mm Innendurchmesser und einigen cm Länge ) wird im
Probenhalter, der in allen drei Raumrichtungen beweglich ist, befestigt und
danach der Probenhalter so lange verstellt, bis die maximale Intensität erreicht
ist (sog. monitoring). Anschließend wird die Justierprobe gegen die zu
untersuchende Probe vertauscht und das Spektrum aufgenommen. Selbstverständlich
muß dabei die Probe die gleichen geometrischen Abmessungen haben. Mit der
Justierprobe wird nur die optimale Position der Probe im Meßraum bestimmt, nicht
aber auf Wellenlängen "geeicht". Wellenlängenkalibrierung wird mit speziellen
Substanzen wie Bariumsulfat vorgenommen. Die heute routinemäßig eingesetzten
Geräte sind in Bezug auf zeitlichen Abweichungen (sog. drifting) sehr stabil.
Abweichung von der Vorgehensweise sind unter Umständen von dem Gerätetyp
abhängig und Details im Handbuch des Geräteherstellers nachzulesen. Obwohl in
der Raman-Spektroskopie temperaturempfindliche und auch farbige Substanzen
vermessen werden können, sind doch zwei Probleme bedeutsam:
Aufheizung der Probe durch die intensive Laserstrahlung (dunkle Proben)
Fluoreszenz der Probe (teilweise oder vollständigen Überlagerung eines Raman-Spektrums)
Durch den heute vorwiegend eingesetzten Neodym-YAG Laser (1060 nm) werden diese Nachteile minimiert.
Wie in der IR-Spektroskopie können aus der Lage der Wellenzahl einer Schwingung auf charakteristische Gruppen im Molekül geschlossen werden. In der Praxis lassen sich auch wegen der sehr geringen Raman-Aktivität von Wasser recht gut wässrige Lösungen untersuchen, wobei allerdings meist eine Bandenverbreiterung der gelösten Probe auftritt. Ein Fall, der den Vorteil der Raman-Spektroskopie gegenüber der IR-Spektroskopie zeigt, ist die Untersuchung von instabilem, hygroskopischem Distickstoffpentoxid (N
2O5), das bei Raumtemperatur merklich sublimiert bzw. zerfällt und zu dem eine hohe Oxidationskraft (Bromid wird sofort zu elementarem Brom oxidiert) besitzt. Durch die unkomplizierte Probenvorbereitung (Vermessung im verschlossenem Glasröhrchen) und die Möglichkeit, den Probenhalter und damit die Probe auf z.B. –60°C zu kühlen, ist dagegen in einigen Sekunde ein gutes Ramanspektrum der Reinsubstanz zu bekommen. Ebenso kann eine Probe in einem heizbaren Probenhalter ( < ca. 180°C) analysiert werden. Die minimal untersuchbaren Mengen sind mit der IR-Spektroskopie zu vergleichen. Die Schwierigkeit einzelne Kristalle von Salzkorngröße zu messen besteht hauptsächlich in der mechanischen Justierung der Probe. Auch können ganze Gegenstände, begrenzt durch den Probenraum und dem Durchmesser des anregenden Laserstrahls (typisch 1 mm Durchmesser, Lage verstellbar), direkt untersucht werden.Leider gibt es zur Zeit im Vergleich zur IR-Spektroskopie wesentlich weniger Literaturspektren und Tabellenwerke. Auch der Einsatz dieser Untersuchungsmethode ist momentan außerhalb von Forschungsstätten noch nicht sehr verbreitet. Eingesetzt wird die Raman-Spektroskopie, wenn auch relativ selten, in vielen Bereichen, unter anderem Pharmazie, Archäologie, Lebensmittelchemie, Pigmentherstellung, Halbleiter- und Sprengstoffuntersuchungen.
![]()
Auf diesem Webangebot gilt die Datenschutzerklärung der TU Braunschweig mit Ausnahme der Abschnitte VI, VII und VIII.