Bei den Atomen genügte uns ein Satz von Quantenzahlen, um die Auswahlregeln für elektronische Übergänge in Gleichungen auszudrücken. Um die Auswahlregeln aufzustellen, mussten wir bei den zweiatomigen Molekülen zusätzlich zu den verfügbaren Quantenzahlen bei heteronuklearen Molekülen noch eine Symmetreieigenschaft (+, −) bzw. bei homonuklearen Molekülen noch zwei Symmetrieeigenschaften (+, -; g, u) der elektronischen Wellenfunktion berücksichtigen.
In nicht-linearen mehratomigen Molekülen verlieren die Quantenzahlen weiter an Bedeutung, da die Symmetrie weiter abnimmt. Eine Ausnahme hierbei bildet der Gesamtspin: Die Auswahlregel
ΔS = 0
gilt nach wie vor, da, solange in dem Molekül nicht ein Atom mit großer Kernladungszahl vorhanden ist, die Spin-Bahn-Wechselwirkung klein ist. So erscheinen z.B. die Singulett-Triplett-Übergänge in Benzol nur schwach im Spektrum, wesentlich intensiver aber im Spektrum des Iodbenzols.
Beim Übergang der Elektronen von einem Molekülorbital zu einem anderen (etwa durch Elektronenanregung in der UV-Spektroskopie) kann man aufgrund der Symmetrie der Orbitale bereits qualitative Aussagen darüber machen, ob der Übergang symmetrie-erlaubt oder symmetrie-verboten ist.
Betrachten wir als erstes Beispiel dazu die Molekülorbitale des trans-Butadiens, die in der schematischen Darstellung wie folgt aussehen:
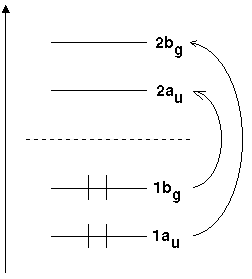
Abb1: MO-Diagramm von Butadien mit irreduzibler
Darstellung der MO's
Die Laporte-Regel besagt nun, dass bei Molekülen, die ein Inversionszentrum besitzen, nur die Übergänge g->u bzw. u->g erlaubt sind.
Da das Übergangsmoment die quantenchemische Größe ist, die eine Aussage über die Intensität eines Elektronenüberganges zuläßt, muss bei einem symmetrieverbotenen Übergang das Übergangsmoment null sein.
Wir wollen dies zunächst prinzipiell behandeln und dann einfache Beispiele angeben, aus denen auch die Lage des Dipolmomentes hervorgeht.
Für einen Übergang zwischen zwei elektronischen Zuständen hängen die Auswahlregeln stark von den Symmetrieeigenschaften ab. (Die Auswahlregeln für elektrische Übergänge in Atomen und zweiatomigen Molekülen können zwar ebenfalls durch Symmetriebetrachtungen abgeleitet werden; es ist aber einfacher, die Quantenzahlen zu verwenden, sofern sie verfügbar sind.)
Die Intensität eines elektronischen Übergangs ist proportional zum Quadrat des Übergangsmomentes |R|², wobei für R gilt:
R = ò y'* µ y'' dτ
Bei einem erlaubten elektronischen Übergang muss |R| ¹ 0 sein. Aus Symmetriegründen muss gelten, dass die Symmetrie des Ausgangszustandes G(y'') in die Symmetrie des Endzustandes G(y') durch das Dipolübergangsmoments G(y) überführt wird. (G(x)steht hier für die Symmetrie eines Objekts x. Es kann also A1, A2, B1 etc. als Wert haben.) So gilt
G(y') x G(µ) x G(y'') = A
G(y') x G(µ) x G(y'') É A
Das Zeichen É bedeutet "enthält". A soll die totalsymmetrische Darstellung einer beliebigen Punktgruppe symbolisieren.
Die Größe R kann in Komponenten entlang der cartesischen Achsen zerlegt werden:
Rx = ò y'* µxy'' dτ
Ry = ò y'* µyy'' dτ
Rz = ò y'* µzy'' dτ
Ein Übergang ist also erlaubt, wenn eine der Komponenten Rx, Ry oder Rz von Null verschieden ist. Wir können als Bedingungen für einen erlaubten Übergang zwischen nicht-entarteten Zuständen daher formulieren:
G(y') x G(Tx) x G(y'') = A
Ist einer der Zustände entartet, müssen wir "=" durch "É" ersetzen. Tx, Ty und Tz sind Translationskomponenten entlang der cartesischen Achsen.
Ist das Produkt zweier irreduzibler Darstellung die totalsymmetrische Darstellung, müssen beide Darstellungen identisch sein. Wir können damit die drei Gleichungen auch anders formulieren:
G(y') x G(y'') = G(Tx) und/oder G(Ty) und/oder G(Tz).
Auch hier ersetzen wir "=" durch "É", wenn ein entarteter Zustand an dem Übergang beteiligt ist. Das ist die allgemeine Auswahlregel für Übergänge zwischen zwei elektronischen Zuständen.
Sind bei einem Übergang auch Schwingungen des Ausgangszustands und/oder des Endzustands beteiligt, müssen wir das elektronische Übergangsmoment R durch das Übergangsmoment Rv ersetzen:
Rv = ò yv'* µyv'' dτv
wobei yv ist eine vibronische Wellenfunktion ist. Mit derselben Argumentationskette wie für einen elektronischen Übergang können wir nun die Auswahlregeln für einen vibronischen Übergang formulieren:
G(yv') x G(yv'') = G(Tx) und/oder G(Ty) und/oder G(Tz).
G(y') x G(yv') x G(y'') x G(yv'') = G(Tx) und/oder G(Ty) und/oder G(Tz).
Das Gleichheitszeichen muss wieder durch "É" ersetzt werden, sobald ein entarteter Zustand an dem Übergang beteiligt ist.
Cs:
Anregung 1A' ↔ 1A''. Um von A' nach A'' zu gelangen (A' Ä ? = A'') muss A'' vorliegen, d.h. µ muss senkrecht zur Molekülebene stehen (µ in Molekülebene hat A'-Symmetrie)C2v:
Anregung 1A1 ↔ 1B1 (A1 Ä ? = B1). Es muss µ B2-Symmetrie aufweisen. Da B2 der y-Richtung entspricht (siehe z.B. H2O das 2py), liegt µ senkrecht zur H2O-Ebene. Die Anregung von 1B1 ↔ 1B2 ist nur über ein Dipolmoment mit A2-Symmetrie möglich. Ein solches gibt es aber nicht, d.h. der Übergang ist verboten.
Durch die asymmetrische Streckschwingung kann diese Übergang jedoch erlaubt sein (die Intensität wird aber schwach sein), denn diese Schwingung verändert die Symmetrie des Moleküls von C2v nach Cs (nur die Molekülebene bleibt als Symmetrie-Element erhalten). Dadurch wird der B2-Zustand zum A' und der B1 zum A''-Zustand. Das Dipolübergangsmoment muss dann A''-Symmetrie aufweisen, also senkrecht zur Molekülebene stehen. Man sieht daran, dass Übergänge möglich werden, wenn die Symmetrie abnimmt.
Auf diesem Webangebot gilt die Datenschutzerklärung der TU Braunschweig mit Ausnahme der Abschnitte VI, VII und VIII.