Unabhängige Teilchen besitzen unterschiedliche "Typen" von Energie.
So kann ein Atom nicht nur Translationsenergie Et sondern auch
elektronische Energie Ee aufweisen. Beispielsweise setzt sich
der Grundzustand eines Halogen-Atom, 2P, aus zwei Komponenten
zusammen, die eine andere Energie und Entartung besitzen, je nach dem wie
der Elektronenspin mit dem elektronischen Drehimpuls wechselwirkt. Beim
Cl-Atom beträgt der energetische Unterschied ΔE
= 880 cm−1.
| niedrigster Zustand (i = 1) | 2P3/2: E1 = 0 cm−1, Entartung g1 = 4 |
| angeregter Zustand (i = 2) | 2P1/2: E2 = 880 cm−1, Entartung g2 = 2 |
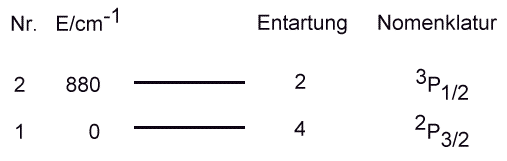 |
| Abb.1: Der elektronische Grundzustand eines Halogen besteht aus zwei Energieniveaus, die unterschiedlich entartet sind. Die rechts angegebene Bezeichnung (Nomenklatur) sagt nichts über die energetischen Verhältnisse aus, wohl aber etwas über die Entartung (g = 2 · Index + 1). Beim Chloratom liegt der erste angeregte Zustand um 880 cm-1 oberhalb des niedrigsten Zustands (E1 = 0 cm-1). |
Ein Molekül kann zusätzlich Rotations- (Er) und Vibrations- (Ev) Energie besitzen. Mit recht guter Näherung können wir all diese Energien als unabhängig von einander ansehen, so dass die Gesamtenergie E eines Teilchens durch
E = Et + Er + Ev + Ee
gegeben ist. Die molekulare Zustandssumme q kann dann geschrieben als
q = Σi,j,k,l [gti grj gvk gel e−(Eti + Erj + Evk + Eel)/kT]
q = Σi,j,k,l [gti e−Eti/kT][grj e−Erj/kT][gvk e−Evk/kT][gel e−Eel/kT]
wobei bespielsweise grJ die Rotationsentartung des j.ten Rotationsniveaus mit der Energie Erj ist. Jede der Summen in der Gleichung hat die Form einer Zustandssumme, so dass wir auch schreiben können:
q = qt · qr · qv · qe
wobei qt = Σi gti e−Eti/kT etc. gilt.
Da immer der Logarithmus von q in den thermodynamischen Funktionen auftritt, können wir sofort feststellen:
ln q = ln qt + ln qr + ln qv + ln qe
Dies bedeutet, dass jede thermodynamische Grösse eines Systems unabhängiger Teilchen als Summe von Translation, Rotation und elektronischem Anteil geschrieben werden kann. Dies hat zur Folge, dass z.B. die innere Energie U als Summe der jeweiligen Beiträge geschrieben werden kann:
U = Ut + Ur + Uv + Ue
Die innere Energie U ist für unterscheidbare und ununterscheidbare Teilchen identisch (gleiches gilt für H, Cv und Cp). Die Entropie S, freie Energie A und freie Enthalpie G hängen jedoch vom Teilchentypus ab und wir bekommen ein Problem bei der Separation von Translation, Rotation, Vibration und elektronischem Beitrag, denn es tritt nun ein Term ln(q/N) anstatt nur ln q auf:
q/N = qt·qr·qv·qe/N = (qt/N) qrqvqe
Da die Translationsbewegung die Teilchen ununterscheidbar macht, wird die Division durch N der Translation zugeschlagen, so dass für die Berechnungen gilt:
ln (q/N) = ln (qt/N) + ln qr + ln qv + ln qe
Z.B. wird der Beitrag der Translation zur Entropie über
| St = Nk {T ∂lnqt/∂T + ln(qt/N) + 1} |
(ununterscheidbare Teilchen) und für die anderen Beiträge
über
| Sr = Nk {T ∂lnqr/∂T + lnqr} |
| Sv = Nk {T ∂lnqv/∂T + lnqv} |
| Se = Nk {T ∂lnqe/∂T + lnqe} |
(unterscheidbare Teilchen) berechnet.
![]()
Auf diesem Webangebot gilt die Datenschutzerklärung der TU Braunschweig mit Ausnahme der Abschnitte VI, VII und VIII.