Am Beispiel der Cyclisierungsreaktion des Butadien
![]()
![]()
Das cis-Butadien ist in der Lage, durch eine Cyclisierungsreaktion Cyclobuten zu bilden:
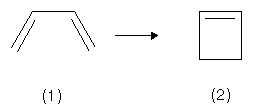
Dabei wird aus den 2 pz-Orbitalen an den Kohlenstoffen 1 und 4 eine σ-Bindung gebildet. Die 2 pz-Orbitale an den Kohlenstoffen 2 und 3 bilden dann die π-Bindung im Cyclobuten. Das π-System im Butadien weist folgendes Knotenverhalten auf:
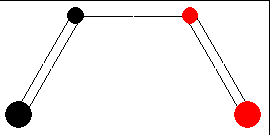 |
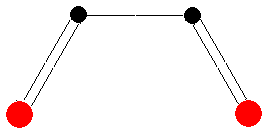 |
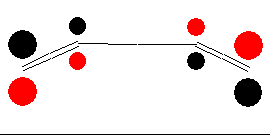 |
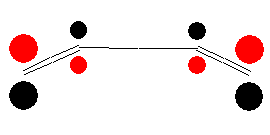 |
| HOMO | LUMO |
Im Grundzustand ist das HOMO mit 2 Elektronen besetzt. Die σ-Bindung kann mit den Elektronen des HOMO's aus den beteiligten Atomorbitalen gebildet werden. Damit es zu einer bindenden Wechselwirkung kommt, muss eine positive Überlappung aus gleichsinnigen Vorzeichen der AO's aufgebaut werden; hierzu müssen sich die Orbitale an beiden Kohlenstoffatomen (1 und 4) gleichsinnig drehen (entweder beide im Uhrzeigersinn, oder beide entgegen dem Uhrzeigensinn).
Somit ergibt sich für die Reaktion (konrotatorisch) etwa folgender Ablauf:
Eine angenommene disrotatorische Cyclisierung würde aus dem HOMO keine bindende Wechselwirkung (Überlappung gleichsinniger Orbital-Vorzeichen) ergeben. Jedoch kann das erst in elektronisch angeregtem Zustand (Photochemie) besetzte LUMO eine bindende sigma-C--C-Bindung knüpfen. Somit ergibt sich für die Reaktion (disrotatorisch) etwa folgender Verlauf:
Die Wechselwirkung der Orbitale (unter Erhalt ihrer Symmetrie) wird in Korrelationsdiagrammen schematisch für den Ablauf der Reaktionen dargestellt.
Auf diesem Webangebot gilt die Datenschutzerklärung der TU Braunschweig mit Ausnahme der Abschnitte VI, VII und VIII.