Bei der Atomspektroskopie entsprechen die Übergänge immer
Änderungen der Elektronenkonfiguration. Bei Molekülen können
zusätzlich noch Schwingungen und Rotationen auftreten, was zur Folge
hat, dass die entsprechenden Spektren (noch) komplizierter als bei
den Atomen sind, dafür aber auch Informationen über Bindungsstärken
und Struktur des Moleküls enthalten.
Wenn wir von isolierten Bewegungsmodi ausgehen, dann ist die Gesamtenergie
E einfach die Summe der elektronischen Eel, der vibronischen
Evib, und der rotatorischen Energie Erot des Moleküls:
Die Energien der Zustände sind deutlich unterschiedlich: hνrot << hνvib << hνel
| νrot | Übergänge zwischen benachbarten Rotationsniveaus | im fernen IR oder Mikrowellen |
| νvib | reine Vibrationsübergänge: | im IR (um 1000 cm-1) |
| νel | elektronische Übergänge | im sichtbaren / UV |
Elektronische Übergänge haben in der Regel auch eine Änderung der Schwingung und Rotation zur Folge. Die erlaubten Übergänge werden durch die Auswahlregeln festgelegt. Für diese elektronischen Übergänge muss das Molekül über kein permanentes Dipolmoment verfügen, da ja das elektrische Feld des absorbierten (oder emittierten) Lichts direkt die Elektronenverteilung "verschieben" kann. Für rovibronische Übergänge innerhalb eines elektronischen Zustandes braucht jedoch das elektrische Feld einen "Angriffspunkt", um einen Übergang einzuleiten, d.h. es ist ein permanentes elektrisches Dipolmoment notwendig (oder es muss durch besondere Umstände induziert werden).
Es sollen zunächst Formeln für die Energieniveaus der Rotation angegeben werden und anhand der Auswahlregeln soll dann das reine Rotationsspektrum analysiert werden. Ist die Energie so hoch, dass eine Schwingung angeregt werden kann, dann werden auch gleichzeitig Rotationen mit angeregt. Ist die Energie noch höher, so dass auch elektronische Zustände angeregt werden können, dann werden i.a. sowohl Schwingungen als auch Rotation angeregt sein. Die Übergangswahrscheinlichkeit von einem Zustand n in einen Zustand m ist allgemein über
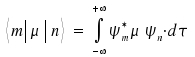
gegeben (dτ ist das Volumenelement) und kann bei Kenntnis von µ und den beiden Wellenfunktionen leicht ausgerechnet werden.
Auf diesem Webangebot gilt die Datenschutzerklärung der TU Braunschweig mit Ausnahme der Abschnitte VI, VII und VIII.